Migliaia di pubblicazioni scientifiche e casi clinici peer-reviewed da consultare
Un recente studio preliminare ha chiarito perché sono stati osservati eventi avversi a seguito di una vaccinazione con RNA messaggero COVID-19 ( mRNA ).
Lo studio , guidato dai ricercatori della Thomas Jefferson University, ha scoperto che le nanoparticelle lipidiche (LNP) utilizzate per trasportare l’mRNA nei vaccini COVID-19 potrebbero “inibire” e “alterare” le risposte immunitarie nei topi.
Gli LNP sono gusci di lipidi vettori dell’mRNA e servono a prevenirne la degradazione e il rilevamento da parte del sistema immunitario del nostro corpo.
Gli LNP non sono mRNA, sono semplicemente un involucro per trasportare il carico di mRNA.
Entrambi i vaccini Pfizer e Moderna mRNA COVID-19 utilizzano LNP per fornire sequenze proteiche spike di mRNA nelle cellule umane. Una volta che le cellule umane hanno ricevuto le sequenze di mRNA, produrranno proteine spike, innescando una risposta immunitaria.
Era previsto che gli LNP fossero innocui nel fornire semplicemente sequenze di mRNA nelle cellule per innescare la produzione di proteine spike e, così facendo, creassero l’immunità contro il virus COVID-19.
Tuttavia, molti studi sui topi da allora hanno scoperto che gli LNP, dichiarati non tossici e sicuri, siano in realtà altamente infiammatori.
Queste nanoparticelle sono altamente resistenti e possono persistere da 20 a 30 giorni nel corpo. Mentre persistono nel corpo, è probabile che continuino ad attivare il sistema immunitario, portando all’esaurimento immunitario e alla non reattività.
Anche lo studio Thomas Jefferson ha condiviso risultati simili. I ricercatori hanno studiato il modo in cui gli LNP influiscono sul sistema immunitario, iniettando nei topi gli stessi LNP usati nei vaccini di Pfizer.
L’infiammazione e le risposte immunitarie nei topi non danno la sicurezza che lo stesso possa accadere negli esseri umani. Tuttavia, i topi sono stati a lungo utilizzati per testare la sicurezza e l’efficacia dei farmaci per uso umano; segni di problemi immunitari sono un’indicazione di possibili rischi per la salute nell’uomo.

(The Epoch Times)
Gli autori hanno scoperto che i topi che avevano ricevuto due dosi avevano una risposta immunitaria ridotta alla loro seconda iniezione rispetto ai topi che avevano ricevuto solo una dose.
“La piattaforma del vaccino mRNA-LNP ( nanoparticelle ) induce cambiamenti immunologici imprevisti a lungo termine che interessano sia le risposte immunitarie adattative che la protezione eterologa contro le infezioni”, scrivono gli autori.
La pre-esposizione alle nanoparticelle di mRNA riduce il numero di cellule innate
I topi a cui erano state iniettate due dosi di LNP avevano un numero ridotto di cellule immunitarie innate, le cellule immunitarie di prima risposta.
Gli autori volevano scoprire come gli LNP, il guscio lipidico che avvolge l’mRNA, influenzasse i topi e per scoprirlo hanno iniettato loro diverse varianti di LNP.
I topi sono stati divisi in tre gruppi, tutti e tre i gruppi hanno ricevuto due iniezioni, anche se con contenuti diversi.
Per la prima iniezione, alla maggior parte dei topi è stata somministrata un’iniezione di LNP. Ad altri sono stati dati LNP contenenti sequenze di mRNA e alla restante parte sono stati dati LNP vuoti senza mRNA all’interno.
Ai topi rimanenti è stata somministrata un’iniezione di soluzione salina. Questi topi sono usati come gruppo di controllo per il confronto, poiché le iniezioni di soluzione salina non dovrebbero introdurre alcun cambiamento nel corpo.
Due settimane dopo, a tutti e tre i gruppi è stata somministrata la stessa iniezione di LNP contenente sequenze di mRNA per una proteina influenzale (HA). La seconda iniezione ha permesso alle loro cellule di produrre proteine HA, che hanno innescato una risposta immunitaria. Era inteso che questa risposta immunitaria avrebbe poi reso i topi immuni al virus dell’influenza.
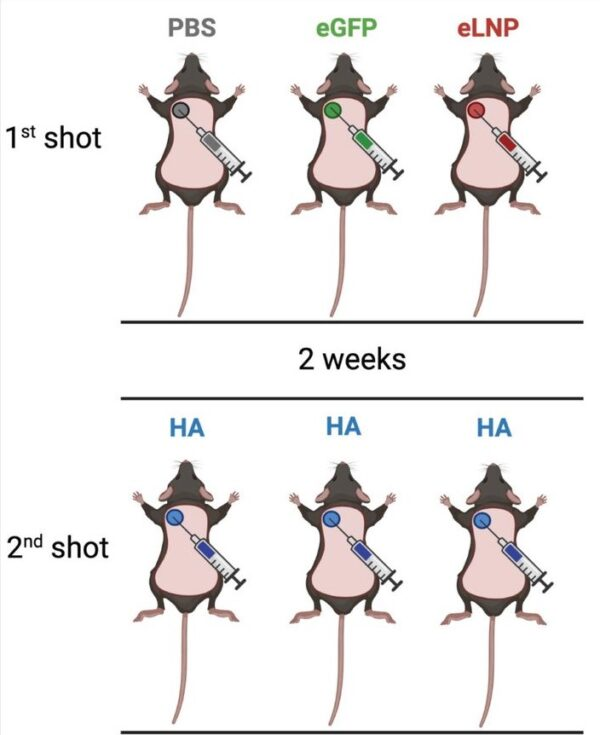
I ricercatori hanno scoperto che dopo la seconda iniezione, tutti i topi avevano sviluppato una difesa immunitaria contro il virus dell’influenza.
Gli autori hanno osservato che i topi a cui erano state somministrate due dosi di LNP erano più resistenti a un’infezione influenzale poiché perdevano meno peso. Stranamente, questi stessi topi avevano anche una risposta immunitaria inferiore al vaccino antinfluenzale con meno cellule immunitarie attivate.
Gli autori hanno ipotizzato che la loro “resistenza” non derivasse probabilmente da un’immunità rafforzata, ma da un prodotto di un percorso alternativo attivato dagli LNP. Non è noto se questa “resistenza” si possa applicare ad altre infezioni o possa essere applicabile solo all’influenza.
Questo perché lo studio ha scoperto che i topi più “resistenti” all’influenza erano in realtà più suscettibili alle infezioni fungine.
I ricercatori hanno infettato i topi con Candida albicans , i topi che avevano ricevuto due dosi hanno perso più peso e avevano un controllo più scarso sull’infezione, indicando un’alterazione della risposta immunitaria innata.
Ulteriori indagini hanno mostrato che questi topi avevano un numero inferiore di neutrofili, che sono le cellule immunitarie di prima risposta più comuni.
Il compito dei neutrofili è pattugliare il corpo e attaccare indiscriminatamente quando rilevano qualcosa di estraneo, quindi un numero ridotto di neutrofili espone un individuo a un rischio maggiore di infezione.
Poiché un’infezione fungina incontrollata, in particolare C. albicans , è spesso un segno di una risposta immunitaria innata o di primo soccorso indebolita, gli autori hanno quindi sospettato che il numero ridotto di neutrofili potesse aver contribuito all’epidemia fungina.
Gli LNP causano infiammazione e alcune vie infiammatorie riducono la produzione di cellule del sangue. Gli autori hanno ipotizzato che le due dosi di LNP che alcuni topi hanno ricevuto potrebbero aver causato una maggiore infiammazione che porta a un calo della produzione di cellule del sangue e a una bassa conta dei neutrofili.
Sebbene si tratti di speculazioni e non sia certo che gli effetti sui topi si applichino all’uomo, ci sono state segnalazioni di casi di insorgenza improvvisa di anemia aplastica grave in individui vaccinati, una condizione in cui l’organismo non riesce più a produrre un numero sufficiente di cellule del sangue, in particolare globuli rossi.
Sono stati inoltre segnalati casi di individui vaccinati con COVID-19 che hanno sviluppato malattie fungine rare e altri con peggioramento di malattie fungine preesistenti.
Sebbene una grave malattia fungina non indichi automaticamente un sistema immunitario debole, tuttavia, gravi infezioni fungine “sono più comuni tra le persone con un sistema immunitario indebolito”, scrive il Centers for Disease Control and Prevention (CDC) degli Stati Uniti .
Numeri di antigeni ridotti nei topi con un’elevata esposizione alle nanoparticelle
All’interno del sistema immunitario, ci sono i primi soccorritori (cellule immunitarie innate) e i secondi soccorritori (cellule immunitarie adattative).
Le cellule di prima risposta sferrano un attacco immediato quando incontrano qualcosa di estraneo. Tuttavia, i loro attacchi sono aspecifici e spesso non riescono a eliminare completamente le infezioni.
Pertanto, le cellule immunitarie adattative, note anche come cellule T e B, fungono da secondi soccorritori.
Vengono attivati circa una settimana dopo l’infezione e eliminano le infezioni montando attacchi potenti e specifici.
Per attivare le cellule immunitarie adattative, le cellule T e B devono ricevere informazioni sull’agente patogeno. Nel caso della Sars-Cov-2, può trattarsi di una sezione della proteina spike.
Le APC (cellule presentanti l’antigene), un tipo di cellula che risponde per prima, portano pezzi di virus, batteri o particelle infettive alle cellule T o B adattative. Questo attiverà le cellule T o B, innescando una risposta immunitaria adattativa.
L’immagine sottostante mostra una cellula dendritica (APC) che attiva una cellula T presentandole un antigene, una sostanza tossica o estranea.
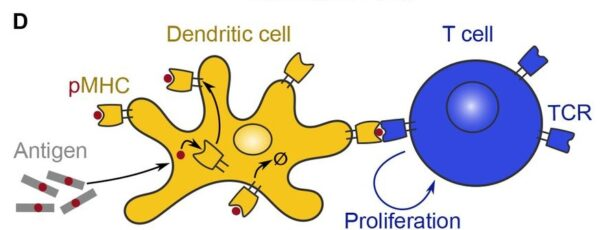
Tuttavia, gli autori hanno riscontrato che i topi a cui erano state somministrate due dosi di LNPs di mRNA presentavano una presentazione dell’antigene ridotta rispetto ai topi a cui era stata somministrata una sola dose di LNPs.
Ciò implica che un minor numero di cellule immunitarie adattative si è attivato contro le proteine dell’influenza.
Le nanoparticelle di mRNA riducono le risposte delle cellule T e B
Gli autori hanno riscontrato che i topi che hanno ricevuto due iniezioni di LNP hanno avuto risposte inferiori delle cellule T e B al vaccino mRNA dell’influenza rispetto ai topi a cui è stata somministrata una sola dose.
Come ultima linea di risposta immunitaria, le cellule T e B sono fondamentali nella capacità del nostro sistema immunitario di eliminare le infezioni.
Tuttavia, gli autori hanno scoperto che i topi a cui erano state somministrate due dosi di LNP di mRNA avevano una presentazione dell’antigene ridotta rispetto ai topi a cui era stata somministrata solo una dose di LNP.
Ciò implica che sono state create meno cellule immunitarie adattative per attivarsi contro le proteine dell’influenza.
Le nanoparticelle di mRNA riducono le risposte delle cellule T e B
Gli autori hanno scoperto che i topi che avevano ricevuto due iniezioni di LNP hanno avuto una risposta inferiore delle cellule T e B al vaccino antinfluenzale mRNA rispetto ai topi a cui è stata somministrata una sola dose.
Come ultima linea di risposta immunitaria, le cellule T e B sono fondamentali nella capacità del nostro sistema immunitario di eliminare le infezioni.
Tuttavia, nei topi a cui sono state somministrate due dosi di LNP, è stata attivata una quantità minore di cellule T e B.
I gruppi a cui è stata somministrata la doppia dose presentavano anche concentrazioni inferiori di anticorpi (le cellule B producono anticorpi) contro la proteina dell’influenza.
La riduzione della risposta immunitaria adattativa era sistemica e persisteva in tutti gli organi e le regioni. Tuttavia, secondo gli autori, questa riduzione era ancora maggiore nel sito di iniezione, soprattutto se i topi venivano sottoposti a iniezioni nello stesso punto per entrambe le punture.
D’altra parte, il gruppo a cui è stata somministrata una sola iniezione di LNP ha avuto risposte più elevate delle cellule T e B, con una maggiore produzione di anticorpi.
Gli autori hanno scoperto che l’esposizione all’LNP ha ridotto le cellule T progenitrici. Poiché le cellule T progenitrici maturano in cellule T attivate, meno progenitori significano una riduzione del numero di cellule T e della risposta, inoltre hanno riscontrato che se le cellule T progenitrici fossero state rimosse prima della vaccinazione e poi reintrodotte dopo la vaccinazione, il numero di cellule T attive non si sarebbe ridotto. Questo suggerisce che le LNP riducono direttamente il numero di cellule T progenitrici e, così facendo, riducono la risposta delle cellule T.
“La pre-esposizione all’mRNA-LNP inibisce la risposta delle cellule T“, scrivono gli autori.
Questa riduzione dell’immunità non dovrebbe essere permanente, hanno ipotizzato gli autori.
Hanno notato che le risposte delle cellule B si sono per lo più ristabilite se è stato introdotto un intervallo di 8 settimane tra la prima e la seconda dose.
Gli autori non hanno verificato il periodo di tempo necessario per un recupero completo, né hanno verificato se la risposta delle cellule B si sia mai ripresa nei topi.
Tuttavia, l’iniezione nei topi di adiuvanti come i sali di alluminio o l’AddaVax ha eliminato gli effetti soppressivi che le iniezioni di LNP avevano sulle loro cellule immunitarie.
“L’inibizione delle risposte immunitarie adattative da parte della pre-esposizione agli mRNA-LNP è duratura, ma è probabile che si affievolisca con il tempo”.
I cambiamenti dell’immunità dovuti agli LNP possono essere ereditati
Come già menzionato, i topi a cui sono state iniettate due dosi di LNP sono risultati più resistenti all’infezione influenzale rispetto ai topi a cui è stata somministrata una sola dose di LNP.
Ciò è stato dimostrato dal maggior mantenimento del peso dei topi durante l’infezione, anche se non è certo che la resistenza sia dovuta a una risposta immunitaria o a qualche altra via innescata dagli LNP.
Stranamente, questa maggiore difensività poteva essere trasmessa alla prole. L’ereditarietà della resistenza contro l’influenza è più forte se entrambi i genitori sono stati immunizzati e meno se lo è un solo genitore, in particolare se solo il genitore maschio è immunizzato.
Tuttavia, lo studio non ha esaminato se la prole erediti anche la debolezza immunitaria, come ad esempio il declino dell’immunità contro il C. albicans, un tratto osservato anche nei topi a cui sono state somministrate due dosi di LNP.
Implicazioni dello studio e domande urgenti
I risultati dello studio sui topi suggeriscono che le funzioni delle cellule T e B sono temporaneamente ridotte nei topi e sollevano la questione se lo stesso avvenga nell’uomo.
La risposta immunitaria adattativa è fondamentale per eliminare le infezioni e prevenire condizioni croniche come il cancro. Lo studio suggerisce che dopo due vaccinazioni con l’mRNA LNPs, i topi presentano alcune settimane di vulnerabilità, che li espone a un rischio maggiore di infezioni e cancro.
Anche negli esseri umani sono state osservate relazioni simili, sebbene non vi siano ancora studi che stabiliscano un legame conclusivo.
Tuttavia, un aumento del tasso di malattie segnalate al Vaccine Adverse Event Reporting System (VAERS) dopo la vaccinazione COVID-19 suggerisce una riduzione dell’immunità nelle persone dopo la vaccinazione.
Sono stati segnalati numerosi casi di tumori in seguito alla vaccinazione con COVID-19.
Nel database VAERS, 284 casi di cancro al seno sono stati segnalati dopo la vaccinazione COVID-19, mentre nell’intera storia del VAERS sono stati segnalati solo 350 casi.
Ci sono stati 269 casi di leucemia segnalati dopo la vaccinazione COVID-19 rispetto ai 432 casi nell’intera storia di VAERS.
Inoltre, sono stati segnalati casi di nuova insorgenza e recidiva dell’herpes zoster in seguito alla vaccinazione con COVID-19. I dati VAERS mostrano che sono stati segnalati 7.559 casi di herpes zoster in seguito alla vaccinazione con COVID-19.
Nell’intera storia di VAERS, sono stati segnalati 28.180 casi di herpes zoster in seguito a qualsiasi vaccinazione, il che significa che circa un quarto dei casi di herpes zoster si sono verificati dopo la vaccinazione con COVID-19.
Il CDC ha indicato che una nuova diagnosi o una recidiva di herpes zoster si verifica principalmente in persone con sistema immunitario compromesso ed è un segno di immunità indebolita.
Sebbene lo studio sui topi suggerisca possibili implicazioni per la salute degli esseri umani, non è noto se tutti i sintomi e gli effetti osservati nei topi si verificheranno nelle persone.
Tuttavia, i dati sempre più numerosi relativi agli effetti avversi sulla salute nell’uomo in seguito alla vaccinazione con COVID-19 giustificano ulteriori ricerche. È inoltre necessario esaminare le sovrapposizioni tra le implicazioni per la salute dei topi e degli esseri umani.
“Considerando l’ampia esposizione di gran parte della popolazione umana ai vaccini basati su questa nuova tecnologia (mRNA), sono necessari ulteriori studi per comprendere appieno i suoi effetti immunologici e fisiologici complessivi. Determinare l’impatto a breve e a lungo termine di questa piattaforma sulla salute umana aiuterebbe a ottimizzarla per ridurne gli effetti potenzialmente dannosi”, hanno concluso gli autori.












