Migliaia di pubblicazioni scientifiche e casi clinici peer-reviewed da consultare
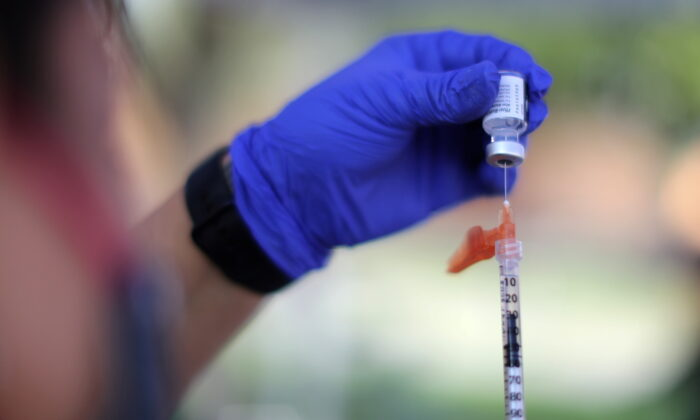
Il richiamo di Pfizer non dovrebbe essere somministrato a coloro che in precedenza hanno ricevuto vaccini prodotti da Moderna o Johnson & Johnson, afferma un alto funzionario sanitario federale.
Doran Fink, vicedirettore della divisione di regolamentazione dei vaccini della Food and Drug Administration(FDA),ha effettuato la valutazione durante un comitato consultivo sui vaccini dei Centers for Disease Control and Prevention (CDC) sull’opportunità che l’agenzia raccomandi una dose aggiuntiva del vaccino Pfizer-BioNTech.
“Non sono disponibili dati per informare l’intercambiabilità di una dose di richiamo di un vaccino con la serie primaria di un altro vaccino”, ha affermato Fink in una riunione del Comitato consultivo del CDC sulle pratiche di immunizzazione il 22 settembre.
In definitiva, la FDA il 22 settembre ha autorizzato i richiami Pfizer per le persone di età pari o superiore a 65 anni e per quelle ad alto rischio di COVID-19, dopo che un comitato consultivo la scorsa settimana ha votato in modo schiacciante contro la somministrazione della terza dose di Pfizer per il pubblico in generale.
La FDA, nel frattempo, ha fatto sapere che necessita di più tempo per stabilire se sono necessarie dosi di richiamo per i vaccini J & J e Moderna.
“Dopo aver considerato la totalità delle prove scientifiche disponibili e le deliberazioni del nostro comitato consultivo di esperti esterni indipendenti, la FDA ha modificato l’EUA per il vaccino Pfizer-BioNTech COVID-19 per consentire una dose di richiamo in alcune fasce di popolazione ha riferito il commissario ad interim della FDA Janet Woodcock durante l’incontro.
Johnson & Johnson questa settimana ha dichiarato che le seconde dosi del suo vaccino hanno aumentato la sua efficacia negli Stati Uniti al 94% contro COVID-19. Il vaccino J & J utilizza un adenovirus, mentre Moderna e Pfizer utilizzano la tecnologia mRNA.
Moderna ha riferito di aver chiesto il permesso di commercializzare terze dosi del vaccino.
La FDA, tuttavia, non ha fornito una tempistica su quando potrebbe prendere una decisione.
Durante la riunione del comitato consultivo della FDA della scorsa settimana sulle dosi di richiamo, alcuni esperti hanno espresso preoccupazione per il fatto che una terza dose di vaccino di Pfizer potrebbe causare effetti collaterali significativi, tra cui la miocardite, nei destinatari più giovani.
“Onestamente non penso che ci siano abbastanza dati di buona qualità a questo punto per prendere una decisione informata”, ha dichiarato Brittany Kmush, epidemiologa della Syracuse University, in riferimento a uno studio israeliano che Pfizer ha citato per affermare che sono necessarie terze dosi negli Stati Uniti, notando il periodo di follow-up di soli12 giorni e la variabilità delle stime degli autori.
Il dottor James Hildreth, un membro votante del gruppo di esperti della FDA, ha aggiunto che nutre “una seria preoccupazione per la miocardite nei giovani”.