Migliaia di pubblicazioni scientifiche e casi clinici peer-reviewed da consultare
L’FDA rilascia un documento “bomba” sul vaccino Pfizer. Così ha intitolato ieri 14 dicembre 2021 “Trial Site News” che su LinkedIn si definisce “il digital media che si occupa al 100% della trasparenza dei trial clinici e della ricerca clinica in tutto il mondo”.
L’inchiesta, a firma di Sonia Elijah, è cosi descritta: “I documenti di Pfizer altamente riservati, sinonimo dell’estrema mancanza di trasparenza avallata dal comportamento delle agenzie governative negli ultimi 20 mesi, hanno portano i critici della narrativa ufficiale a chiedere “mostrateci i dati” e ora vengono finalmente rivelati – beh, in un certo senso non tutti, solo le prime centinaia di pagine su 451.000 presentate da Pfizer”.
E’ stata depositata, ai sensi della normativa cosiddetta FOIA (Freedom of Information Act), il 27 agosto scorso la richiesta per accedere a tutta la documentazione Pfizer su cui la FDA aveva fatto affidamento per autorizzare il vaccino Pfizer-BioNTech Covid-19 in uso emergenziale. L’agenzia che ha ricevuto una richiesta FOIA è tenuta a “determinare entro 20 giorni lavorativi dal ricevimento di tale richiesta se conformarsi a tale richiesta” , come stabilito dalla legge FOIA del 1967. La FDA ha impiegato tre mesi per pubblicare le prime 91 pagine redatte, il 20 novembre scorso.
La richiesta FOIA è stata emessa da un gruppo di oltre 30 scienziati e accademici che hanno intentato una causa civile contro la FDA perché non hanno pienamente ottemperato alla richiesta, ma è stato rilasciato meno dell’1% della documentazione e la FDA che ha preso la dichiarato che tutti i dati sarebbero stati condivisi entro il 2076.
Successivamente, la stessa FDA ha affermato che verranno condivisi entro il 2096, poichè era emersa l’esistenza di migliaia di pagine aggiuntive, per un totale di 451.000 contro le 320.000 pagine originariamente dichiarate. Tuttavia, la velocità con cui la FDA è disposta a rilasciare la documentazione non è cambiata e rimane di 500 pagine al mese. Vale la pena notare, però, che la FDA ha impiegato solo 108 giorni per studiare e approfondire le 451.000 pagine rilasciate da Pfizer prima di autorizzare il vaccino Pfizer BNT162B2 per l’uso dell’autorizzazione di emergenza il 1 dicembre 2020.
Gli scienziati, i funzionari della sanità pubblica e gli accademici, guidati dal noto cardiologo dottor Peter McCullough, hanno formato il gruppo di ricorrenti, il PHMPT (Public Health and Medical Professionals for Transparency), rappresentati dallo studio legale newyporkese di Aaron Siri, di Siri & Glimstad LLP.
In un’intervista esclusiva con Trial Site News , Aaron Siri, socio amministratore dello studio legale, che ha una vasta esperienza nel contenzioso civile, ha dichiarato:
“Il tribunale non ha ancora ordinato la produzione di una sola pagina. Per la maggior parte dei casi, quando la nostra società invia una richiesta FOIA, i documenti vengono subito rilasciati ma la FDA vuole farlo a un ritmo incredibilmente lento, non commisurato alle esigenze della richiesta. Il problema non è se lo produrranno, poichè lo produrranno. Il punto è quanto tempo ci vorrà e poi una volta ottenuto il materiale analizzeremo tutte le note che hanno inserito”.
Quando è stato chiesto se verranno fatte richieste FOIA per ottenere la documentazione di Moderna e Janssen (società del gruppo Johnson&Johnson) fornita alla FDA per ottenere l’autorizzazione all’uso di emergenza, ha risposto:
“Non si può fare una richiesta fino a quando un vaccino non sia stato autorizzato. L’autorizzazione per l’uso di emergenza non è la stessa cosa della licenza o dell’approvazione. Il vaccino Pfizer è l’unico vaccino che è stato autorizzato/approvato come “sicuro ed efficace” secondo la FDA il 23 agosto 2021“.
I dettagli sul caso e i relativi documenti giudiziari possono essere letti sul blog dell’avvocato Aaron Siri, Injecting Freedom .
Le prime centinaia di pagine dei documenti Pfizer appena rilasciati sono state condivise sul sito web del gruppo dei ricorrenti, il PHMPT.
Il fulcro di questo report investigativo è incentrato sul documento di 38 pagine , intitolato ” Analisi cumulativa dei rapporti di eventi avversi post-autorizzazione di PF-07302048 (BNT162B2) ricevuti fino al 28 febbraio 2021 “. Il report è stato redatto da Pfizer, tra il 1 dicembre 2020 e il 28 febbraio 2021. Le segnalazioni di eventi avversi provengono da Stati Uniti, Regno Unito, Italia, Germania, Francia, Portogallo, Spagna e altri 56 paesi.
È interessante notare che il documento rappresenta un’analisi modificata fornita da Pfizer, una risposta ai loro fallimenti associati alla presentazione incompleta di un pacchetto di dati sulla sicurezza alla FDA, che l’agenzia ha commentato. Viene fatto riferimento alla richiesta della FDA del 9 marzo a Pfizer. Si legge nel documento: “Siamo molto interessati a un’analisi cumulativa dei dati sulla sicurezza post-autorizzazione per supportare la vostra futura presentazione di BLA (“Biologics license application”- Richiesta di commercializzazione del vaccino)”. Inviate un’analisi integrata dei vostri dati cumulativi sulla sicurezza post-autorizzazione, inclusa l’esperienza post-autorizzazione negli Stati Uniti e all’estero, nella vostra prossima presentazione BLA. Includete un’analisi cumulativa dei rischi importanti identificati, dei rischi potenziali importanti e delle aree di informazioni mancanti importanti identificate nel vostro Piano di Farmacovigilanza, così come gli eventi avversi di particolare interesse e gli errori di somministrazione del vaccino (associati o meno a un evento avverso). Includete anche i dati di distribuzione e un’analisi degli eventi avversi più comuni. Inoltre, si prega di inviare il piano di farmacovigilanza aggiornato con la richiesta di BLA“.
Nel breve periodo di tre mesi in cui i dati sono stati “riportati spontaneamente a Pfizer”, sono stati registrati 42.086 casi con 158.893 eventi. Secondo i dati, si può interpretare che ogni soggetto in media (caso) avrebbe sofferto di poco meno di quattro sintomi (eventi). Particolarmente preoccupante è che la FDA ha scelto di proteggere gli interessi di Pfizer oscurando il numero totale di dosi, ostacolando la possibilità di calcolare i tassi di incidenza e fornire un’analisi significativa dei dati. Un altro fatto profondamente preoccupante è incentrato su importanti limitazioni citate da Pfizer: “l’entità della sottostima è sconosciuta”. In relazione a questo argomento, i ricercatori hanno condotto un importante studio di Harvard condotto dal 2007-2010, ha scoperto che “meno dello 0,3% di tutti gli eventi avversi da farmaci e l’1-13% degli eventi gravi vengono segnalati alla FDA”. Supponendo che questo calcolo sia corretto, possiamo concludere che i 42.086 casi rappresentano un importo incredibilmente sottostimato.
Altre “incognite” significative disseminate nell’analisi di Pfizer sono:
- 2990 casi in cui il sesso è sconosciuto
- 6876 casi in cui l’età è sconosciuta
- 9440 casi in cui i risultati sono sconosciuti
Un’altra anomalia che spicca è che per gli esiti dei casi, Pfizer ha scelto di includere coloro che si stanno riprendendo da eventi avversi nella stessa categoria con quelli guariti, sotto l’etichetta ” Recuperati/Ristabiliti” . Questa classificazione unitaria sembra discutibile.
Il gran numero di segnalazioni spontanee di eventi avversi
L’analisi prende atto, con allarme, del fatto che ci sia stato un volume così grande di eventi avversi, classificati come “casi gravi” in quel breve periodo di tempo, tanto che Pfizer ha dovuto assumere più dipendenti a tempo pieno e determinare nella tecnologia significative modifiche per far fronte all’elaborazione delle segnalazioni numerose rispettando anche le tempistiche di segnalazione cosi come regolamentato. Come segnalato nel documento:
“A causa dell’elevato numero di segnalazioni spontanee di eventi avversi ricevuti per il prodotto, il titolare dell’autorizzazione all’immissione in commercio ha dato la priorità all’elaborazione dei casi gravi, per rispettare le tempistiche di segnalazione accelerate, come regolamentato, e garantire che queste segnalazioni siano disponibili per il rilevamento del segnale e l’attività di valutazione.” Il rapporto ha proseguito descrivendo come Pfizer abbia gestito questo gran numero di segnalazioni di eventi avversi. ‘ Pfizer ha inoltre intrapreso molteplici azioni per contribuire ad alleviare il grande aumento delle segnalazioni di eventi avversi. Ciò include miglioramenti tecnologici significativi e soluzioni di processo e flusso di lavoro, oltre all’aumento del numero di colleghi per l’immissione di dati e l’elaborazione dei casi. Ad oggi, Pfizer ha assunto ulteriori dipendenti b4 a tempo pieno (FTE)..’
I 1228 decessi
All’interno del documento prodotto da Pfizer, emerge un dato grave mai trasmesso: sono state registrate 1228 morti entro tre mesi dall’assunzione del vaccino, mentre nessun dato riporta il genere dei partecipanti allo studio deceduti. Questi dati, che hanno significative implicazioni sulla sicurezza, erano noti a Pfizer entro la fine di febbraio, ma il 12 aprile, il dottor Mace Rothenberg, ex direttore medico di Pfizer, parlando con il Washington Journal dello sviluppo del vaccino Pfizer, ha dichiarato: “Posso dire che non sono stati negati i dati” e “non ci sono stati morti che si sono verificati direttamente a causa del solo vaccino”. Coloro che difendono la sicurezza del vaccino Pfizer hanno detto che “la correlazione non implica causalità, in cui due eventi che si verificano insieme non stabiliscono una relazione causa-effetto.
La pagina 10 dell’analisi Pfizer presenta un importante rischio identificato di anafilassi con nove decessi segnalati. Quattro su nove si sono verificati lo stesso giorno in cui gli individui sono stati vaccinati.
Pfizer ha sottolineato che questi individui avevano morbilità pregresse, ma il fatto che tutte e quattro sono morte lo stesso giorno in cui hanno ricevuto il vaccino, suggerisce una potenziale causalità di morte con causa vaccinale.
Nella Tabella 7 delle pagine 16-17, sono stati riportati 1403 casi di AESI cardiovascolari (Adverse Event of Specific Interest -Evento avverso di interesse specifico) e classificati come segue: Aritmia; insufficienza cardiaca ; Insufficienza cardiaca acuta; Shock cardiogenico; Coronaropatia; Infarto miocardico; Sindrome da tachicardia posturale ortostatica; cardiomiopatia da stress; Tachicardia.
La latenza di insorgenza dell’evento rilevante variava da meno di 24 ore a 21 giorni. Ciò significa che gli eventi rilevanti si sono verificati da un periodo inferiore a 24 ore fino a 21 giorni dalla somministrazione del vaccino, con una mediana inferiore a 24 ore. 136 eventi rilevanti sono stati fatali. Pertanto, il 50% di questi esiti rilevanti (inclusi i decessi) si è verificato meno di 24 ore dalla somministrazione del vaccino. Questo indica ancora una volta la causalità della morte del vaccino.
Tuttavia, Pfizer in qualche modo conclude: “Questa revisione cumulativa dei casi non solleva nuovi problemi di sicurezza. La sorveglianza continuerà».
Quando si esamina la categoria “AESI immunomediati/autoimmuni”, sono stati segnalati 1050 casi, con le donne colpite poco più di tre volte rispetto agli uomini: ci sono stati 12 esiti fatali. La mediana della latenza di insorgenza dell’evento rilevante era inferiore a 24 ore, il che suggerisce ancora una volta la causalità della morte del vaccino.
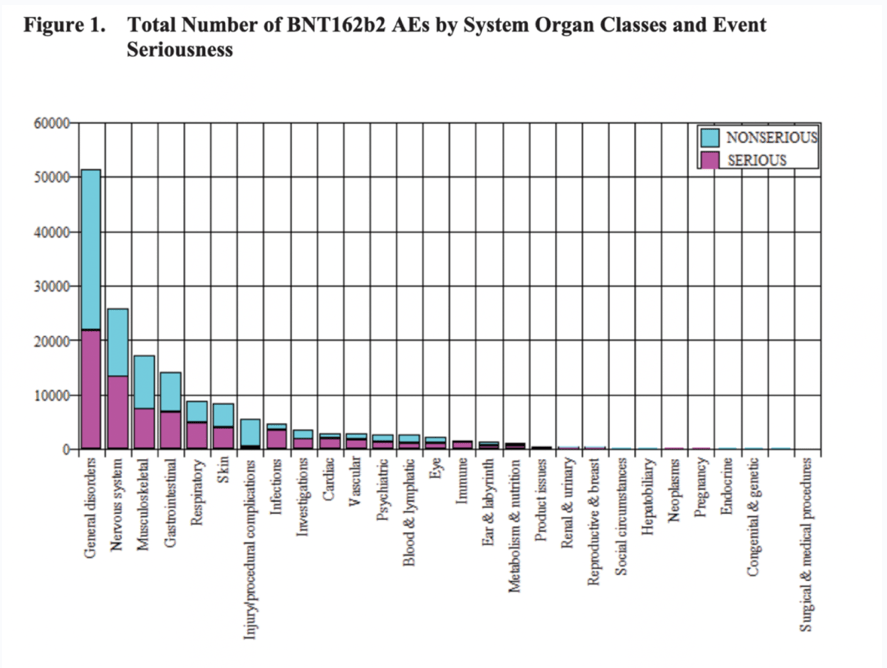
La gravità dei casi
Osservando il grafico sottostante, una parte significativa dei casi viene segnalata come grave rispetto a quella non grave con il maggior numero di casi gravi nella categoria “disturbi generali”. Un caso grave è un caso clinicamente significativo che porta al ricovero in ospedale o che ha una conseguenza con pericolo di vita o la morte. È interessante notare che i casi cardiaci, immunitari, vascolari e le infezioni sono in gran parte casi gravi e per i casi immuni sono tutti classificati come gravi.
Le donne sono per tre volte più colpite dagli eventi avversi del vaccino.
In generale, in ogni categoria di AESI (eventi avversi di particolare interesse), le donne sono state generalmente tre volte più colpite rispetto agli uomini. Tuttavia, da nessuna parte questo è stato così evidente come nel caso dell’anafilassi (una reazione allergica potenzialmente pericolosa per la vita), in cui le donne erano oltre otto volte più colpite. Dei 1002 casi di anafilassi segnalati che soddisfacevano il livello di Brighton Collaboration di 1-4 (il livello 1 è il più alto livello di certezza diagnostica dell’anafilassi) 876 donne sono state colpite rispetto a 106 uomini. Le donne erano anche significativamente più colpite da eventi cardiovascolari con 1076 casi rispetto a 291 casi che hanno colpito gli uomini. I dati statisticamente significativi rivelano la reale possibilità di rischi per la sicurezza dei vaccini specifici per genere.
Tuttavia, da nessuna parte nell’analisi di Pfizer l’azienda commenta questi dati, ma riafferma invece con sicurezza che “la revisione cumulativa dei casi non solleva nuovi problemi di sicurezza”.
Le informazioni mancanti
Degno di nota, inoltre, il fatto che i dati associati all’“Uso in gravidanza e allattamento” siano stati in qualche modo esclusi nell’analisi originale presentata alla FDA. Nella versione modificata vengono segnalati 413 casi avversi di cui 84 classificati come gravi.
Gli esiti della gravidanza per le 270 gravidanze sono stati riportati come aborto spontaneo (23), esito in sospeso (5), parto prematuro con morte neonatale, aborto spontaneo con morte intrauterina (2 ciascuno), aborto spontaneo con morte neonatale e esito normale (1 ciascuno) .
È allarmante che Pfizer affermi che ” non sono emersi segnali di sicurezza dalla revisione di questi casi di utilizzo in gravidanza e durante l’allattamento”. I dati contenuti nel documento redatto sembrano contraddire questa valutazione ottimista.
Nei soggetti pediatrici di età < 12 anni, per i quali originariamente mancava dall’analisi di Pfizer, sono stati segnalati 34 casi di cui 24 classificati come gravi. Il fatto che ai bambini piccoli sia stato somministrato il vaccino Pfizer desta preoccupazione poiché l’autorizzazione all’uso di emergenza non era stata concessa all’azienda per la somministrazione alla popolazione pediatrica in quel momento. Inoltre, la fascia d’età ha destato notevole allarme dato che le somministrazioni hanno coperto un’età ‘ da 2 mesi a 9 anni ‘. Il report manca di dati su quanti bambini in totale hanno ricevuto il vaccino, quindi non c’è modo di calcolare i tassi di incidenza per estrapolare un’analisi significativa.
Un elenco degli eventi avversi noti nell’analisi cumulativa di Pfizer.
Patologie del sistema emolinfopoietico : linfoadenopatia
Eventi cardiovascolari : infarto miocardico acuto; aritmia; Insufficienza cardiaca; Insufficienza cardiaca acuta; Shock cardiogenico; Coronaropatia; Infarto miocardico; Sindrome da tachicardia posturale ortostatica; cardiomiopatia da stress; Tachicardia
Disordini gastrointestinali
Patologie generali e disturbi relativi alla sede di somministrazione
Infezioni
Patologie del sistema muscoloscheletrico e del tessuto connettivo : artralgia; Artrite; artrite batterica; Sindrome dell’affaticamento cronico; poliartrite; polineuropatia; Sindrome da stanchezza post virale; Artrite reumatoide
Patologie del sistema nervoso
Patologie respiratorie, toraciche e mediastiniche: infezioni del tratto respiratorio inferiore; insufficienza respiratoria, infezioni virali del tratto respiratorio inferiore; sindrome da distress respiratorio acuto; Intubazione endotracheale; ipossia; Emorragia polmonare; disturbo respiratorio; Grave sindrome respiratoria acuta
Patologie della cute e del tessuto sottocutaneo
Anafilassi
Malattia potenziata associata al vaccino (VAED) inclusa la malattia respiratoria potenziata associata al vaccino (VAERD).
COVID-19
Paralisi facciale
Disturbi immunomediati/autoimmuni
Neurologico (compresa demielinizzazione): Convulsioni; Atassia; cataplessia; encefalopatia; fibromialgia; La pressione intracranica è aumentata; Meningite; Meningite asettica; narcolessia
Correlati alla gravidanza : infezione della cavità amniotica; Taglio cesareo; anomalia congenita; Morte neonatale; eclampsia; Sindrome da sofferenza fetale; Bambino di basso peso alla nascita; Esposizione materna durante la gravidanza; Placenta previa; pre-eclampsia; Parto prematuro; Nato morto; Rottura uterina; Vasa praevia
Renale: danno renale acuto, insufficienza renale
Eventi tromboembolici: Embolia e trombosi; AESI ictus, Trombosi venosa profonda; Coagulazione intravascolare disseminata; Embolia; Embolia venosa; Embolia polmonare
Vale la pena confrontare l’elenco di cui sopra con l’elenco di seguito accessibile tramite il sito Web della FDA sotto il documento “Scheda informativa Pfizer-BioNTech per destinatari e operatori sanitari”, rivisto il 9 dicembre 2021. È evidente che molti dei eventi gravi e a rischio vita non sono stati inclusi, anche se l’analisi cumulativa di Pfizer delle segnalazioni di eventi avversi post-autorizzazione è stata prodotta per la FDA il 30 aprile 2021.
Download












